食品科学技术及工业的发展和贸易全球化促进了中国市场上食品来源的多样性。其中较为明显的趋势便是食品及原料的供应日益全球化,食品原料的种类和来源也随之不断扩大,一些在中国没有传统食用习惯的食品原料也逐渐进入消费者的视野。为了规范食品原料的开发和应用,保障食品安全,这些原料在进入市场销售前必须要进行新食品原料的申报与评估,经国家卫生健康委员会(下文简称为卫健委)批准,才可进行销售。为促进各企业对新食品原料的了解,避免出现食品合规性问题,此简介对中国新食品原料管理制度进行了介绍。
一、 新食品原料介绍
新食品原料这一名词的前身为新资源食品,最初来源于1983年中国颁布的《食品卫生法(试行)》其中第二十二条规定(“利用新资源生产的食品必须经卫生部门审批”),由此初步确定了新资源食品的基本管理制度。此后,2009年颁布实施的《食品安全法》第四十四条中则使用了“新的食品原料”这一表述。2013年,随着《新食品原料安全性审查管理办法》的颁布实施,“新资源食品”正式更名为“新食品原料”并延续使用至今。目前现行的《新食品原料安全性审查管理办法》已实施将近13年之久,预测未来新食品原料相关的法规也将进行整改修订,进一步明确细化管理制度及法规内容,查缺补漏。
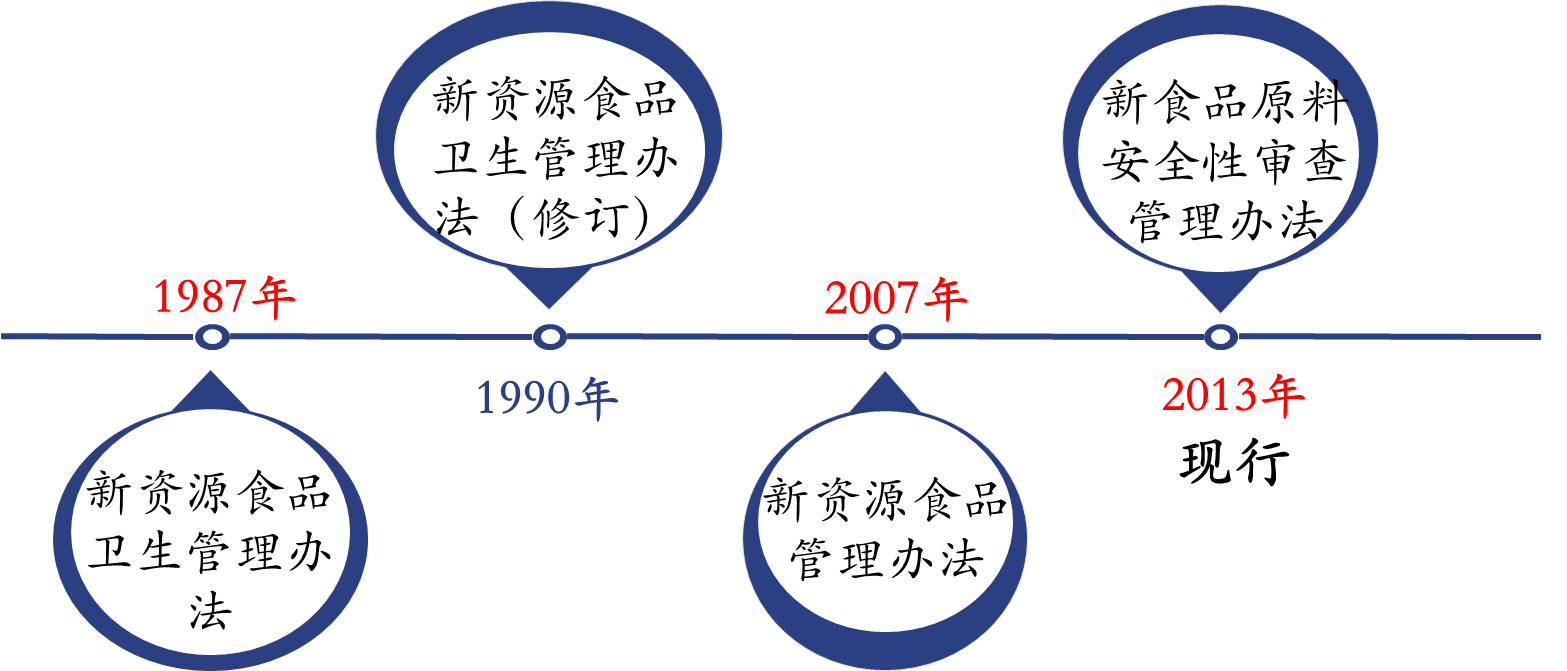
来源:中食安信
图1:新食品原料法规发展进程
自1987年至2007年,食品终产品和食品原料均可以按照新资源食品划分,随着管理规定的更新,自2007年12月起,此类规定的管理对象被限定在食品原料方面,此外,对此类原料的定义和范围也逐渐明确并细化。同时,随着相关管理规定的完善,现行有效的《新食品原料安全性审查管理办法》还明确了不符合申报要求的4种非新食品原料:1. 不具有食品原料特性的物质;2. 已列入GB 2760和GB 14880的物质(即食品添加剂和营养强化剂);3. 国家卫健委已作出不予行政许可的物质;4. 其他不符合有关法律法规规定的物质。
就批准情况来看,自2008年至2019年,公告批准的新食品原料总数为130个(具体情况见图2,具体批准原料列表见表1)。
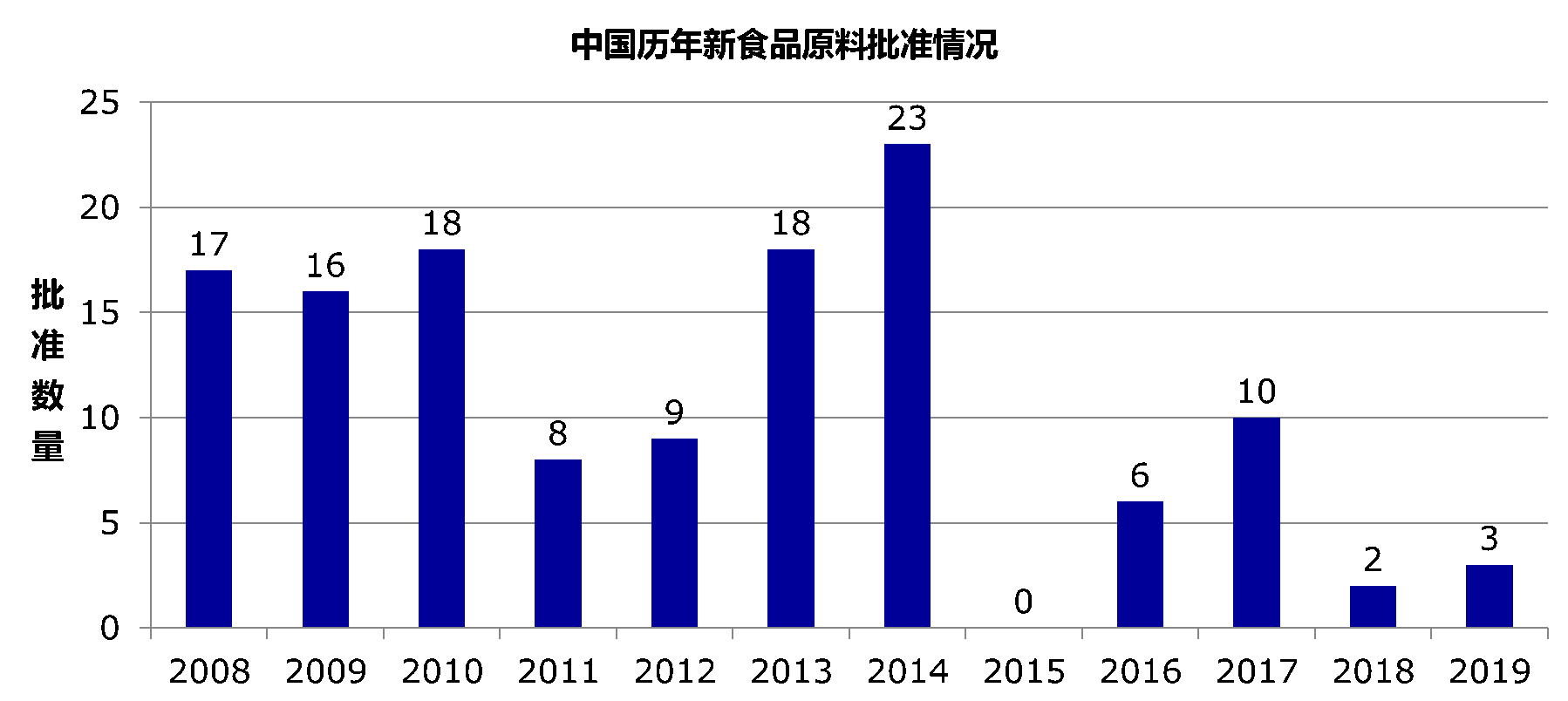
来源:中食安信
图2:中国历年新食品原料批准情况
表1:中国历年批准的新食品原料列表
年份 | 新食品原料名称 |
2008 | 嗜酸乳杆菌(菌株号:DSM13241)、透明质酸钠、叶黄素酯、L-阿拉伯糖、短梗五加、库拉索芦荟凝胶、低聚半乳糖、副干酪乳杆菌(菌株号:GM080、GMNL-33)、嗜酸乳杆菌(菌株号:R0052)、鼠李糖乳杆菌(菌株号:R0011)、水解蛋黄粉、异麦芽酮糖醇、植物乳杆菌(菌株号:299v)、植物乳杆菌(菌株号:CGMCC NO.1258)、植物甾烷醇酯、低聚木糖、珠肽粉 |
2009 | 蛹虫草、菊粉、多聚果糖、γ-氨基丁酸、初乳碱性蛋白粉、共轭亚油酸、共轭亚油酸甘油酯、植物乳杆菌(菌株号:ST-Ⅲ)、杜仲籽油、茶叶籽油、盐藻及提取物、鱼油及提取物、甘油二酯油、地龙蛋白、乳矿物盐、牛奶碱性蛋白 |
2010 | DHA藻油、棉子低聚糖、植物甾醇酯、植物甾醇、花生四烯酸油脂、白子菜、御米油、金花茶、显脉旋覆花(小黑药)、诺丽果浆、酵母β-葡聚糖、雪莲培养物、蔗糖聚酯、玉米低聚肽粉、磷脂酰丝氨酸、雨生红球藻、表没食子儿茶素没食子酸酯、费氏丙酸杆菌谢氏亚种 |
2011 | 翅果油、β-羟基-β-甲基丁酸、元宝枫籽油、牡丹籽油、玛咖粉、乳酸乳球菌乳酸亚种、乳酸乳球菌乳脂亚种、乳酸乳球菌双乙酰亚种 |
2012 | 蚌肉多糖、中长链脂肪酸、小麦低聚肽、人参(人工种植)、蛋白核小球藻、乌药叶、辣木叶、蔗糖聚酯、肠膜明串珠菌肠膜亚种 |
2013 | 茶树花、盐地碱蓬籽油、美藤果油、盐肤木果油、广东虫草子实体、阿萨伊果、茶藨子叶状层菌发酵菌丝体、裸藻、1,6-二磷酸果糖三钠、丹凤牡丹花、狭基线纹香茶菜、长柄扁桃油、光皮梾木果油、青钱柳叶、低聚甘露糖、显齿蛇葡萄叶、磷虾油、马克斯克鲁维酵母 |
2014 | 壳寡糖、水飞蓟籽油、柳叶蜡梅、杜仲雄花、线叶金雀花、塔格糖、奇亚籽、圆苞车前子壳、罗伊氏乳杆菌(菌株号:DSM17938)、蛹虫草、植物甾烷醇酯、茶叶茶氨酸、番茄籽油、枇杷叶、阿拉伯半乳聚糖、湖北海棠(茶海棠)叶、竹叶黄酮、燕麦β-葡聚糖、清酒乳杆菌、产丙酸丙酸杆菌、低聚木糖(调整)、乳酸片球菌、戊糖片球菌 |
2015 | 无 |
2016 | 肉葡萄球菌、发酵乳杆菌(菌株号:CECT5716)、短双歧杆菌(菌株号:M-16V)、凝结芽孢杆菌、小牛葡萄球菌、木糖葡萄球菌 |
2017 | 乳木果油、(3R,3'R)-二羟基-β-胡萝卜素、宝乐果粉、N-乙酰神经氨酸、顺-15-二十四碳烯酸、西兰花种子水提物、米糠脂肪烷醇、γ-亚麻酸油脂(来源于刺孢小克银汉霉)、β-羟基-β-甲基丁酸钙、木姜叶柯、 |
2018 | 黑果腺肋花楸果、球状念珠藻(葛仙米) |
2019 | 弯曲乳杆菌、明日叶、枇杷花 |
二、新食品原料申报材料要求
如果企业使用的原料符合新食品原料的定义,则在使用前需将原料申报为新食品原料。根据《新食品原料申报与受理规定》的要求,申请新食品原料所需的材料有以下内容(具体细节要求需根据不同原料的种类而定):
(1)申请表
(2)新食品原料研制报告
(3)安全性评估报告
a) 成分分析报告
b) 卫生学检验报告(有资质要求)
c) 毒理学评价报告
(有资质要求,试验项目根据国内外使用情况而定,项目数波动范围为2~7项)
d) 微生物耐药性试验和产毒能力试验(有资质要求,仅针对微生物)
e) 安全性评估意见
(需提供申报物质基本信息、成分分析、毒理学资料、人群资料、食用和使用情况和摄入量评估等信息给符合资质要求的机构撰写)
(4)生产工艺
(5)执行的相关标准
(6)标签及说明书
(7)国内外研究利用情况和相关安全性评估资料
(8)申报委托书(委托代理申报时提供)
(9)有助于评审的其他资料
(10)未启封最小包装的样品1件或者原料30克
此外,申报物质为进口的情况下,还需提供以下文件:
(11)进口新食品原料需提交的材料
a) 进口新食品原料出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料
b) 进口新食品原料生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料
三、新食品原料审批流程
新食品原料的具体审批流程可见图3。
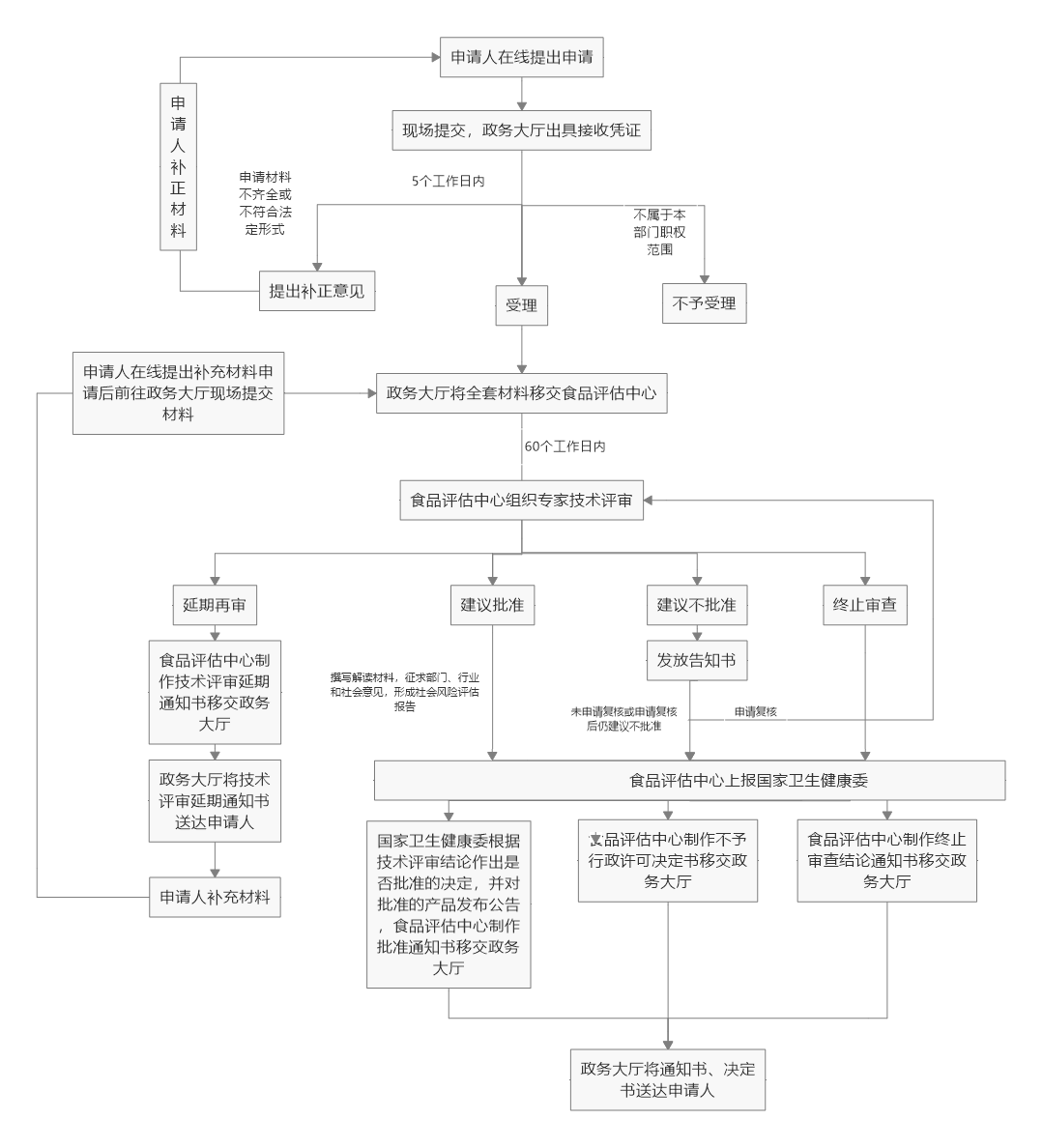
来源:参照卫健委官网
图3:新食品原料审批行政许可工作流程图
四、审评结论
由图3可知,新食品原料的审查结论分为4种情况,分别为延期再审、建议批准、建议不批准和终止审查,对于这些情况的具体说明如下:
延期再审
如果提交的申报材料有需要修改、补充的内容,或是需要进一步进行验证性试验或科学论证的情况,卫健委会出具“行政许可技术评审延期通知书”,申请人需根据通知书内容,补充提交缺少的申报材料,再进行一次专家审评。
建议批准
如果申报物质通过专家组织的审评且结论为“建议批准”,卫生健康会员会会面向社会征求意见,征求意见时间为30日。此后,卫健委会对征求的意见进行研究,最后由卫健委出具“行政许可审查结论通知”。
建议不批准
如果申报的物质出现不符合新食品原料定义(比如不具有食品原料特性),或不符合应当有的营养要求,或安全性不能保证等情况,技术评审结论会为“建议不批准”。卫健委会向申请人出具“行政许可技术评审意见告知书”。如果申请人对此结论有异议,可在30日内提出复核申请,如复核后结论仍为“建议不批准”或逾期未提出复核申请的,则卫健委会像申请人出具“不予行政许可决定书”,并告知不予许可的理由。
需要注意的是,如果申报材料或样品不真实也会造成“建议不批准”的情况。此外,按照上文非新食品原料的定义,不予行政许可的物质不能再次申报新食品原料。
终止审查
如果申报的物质为普通食品原料,或与普通食品原料或已批准的新食品原料实质等同,则卫健委会会向申请人出具“行政许可终止审查通知书”,并告知终止审查的理由。
实质等同一词出自于2007年的《新资源食品管理办法》,是指如某个新申报的食品原料与食品或者已公布的新食品原料在种属、来源、生物学特征、主要成分、食用部位、使用量、使用范围和应用人群等方面相同,所采用工艺和质量要求基本一致,可以视为它们是同等安全的,具有实质等同性。
五、参考法规
《食品安全法》
《新资源食品管理办法》
《新食品原料安全性审查管理办法》
《新食品原料申报与受理规定》
《新食品原料安全性审查规程》
新食品原料申报可行性评估及新食品原料的全程代理审报服务
新食品原料的申报过程较为复杂,审批周期相对较长,注册过程中需提供的申报材料和补正材料等均有严格的要求,对企业来说需要有专门的团队或人员配合,企业需提前做好充分准备。中食安信可提供新食品原料申报可行性评估服务,以及新食品原料的全程代理审报服务,提高企业申报效率,降低人力、资金成本。有任何问题欢迎随时联系我们(010-51301566)。












 京公网安备11010502045875
京公网安备11010502045875