自2023年10月起,由国家市场监督管理总局发布的多项法规、标准以及地方标准即将实施。其中,国家市场监督管理总局发布的《保健食品原料目录 营养素补充剂(2023年版)》《允许保健食品声称的保健功能目录 营养素补充剂(2023年版)》和《保健食品原料目录 大豆分离蛋白》《保健食品原料目录 乳清蛋白》的公告及《婴幼儿配方乳粉产品配方注册管理办法》,均将于2023年10月1日正式实施。
为了更好的帮助企业了解重要法规情况,中食安信对相关内容进行了简单解读,供大家参考。
一、《保健食品原料目录 营养素补充剂(2023年版)》等四个保健食品目录自本月起实施
国家市场监管总局会同国家卫生健康委、国家中医药管理局制修订并发布了四个保健食品目录。其中《保健食品原料目录营养素补充剂(2023年版)》与2020年版相比,增加了“钙、铁、维生素k”等营养素类别下的化合物及标准依据,如“酪蛋白磷酸肽+钙”、“氯化高铁血红素”、“维生素K2(合成法)”;新增了营养素“二十二碳六烯酸(DHA)”,功效为“补充n-3多不饱和脂肪酸”,适宜人群为成人,来源为“二十二碳六烯酸油脂”,附录列明了“DHA藻油原料技术要求”。
本次将“大豆分离蛋白”与“乳清蛋白”共2种原料列入《保健食品原料目录》,确定了符合相应原料目录信息的产品可以纳入备案管理,功效为“增强免疫力”,用量范围6-25g、适宜人群“因蛋白质摄入不足而致免疫低下的成人”、不适宜人群“少年儿童”、备案剂型为“粉剂”,原料技术要求规定,不得以水解等方式改变原料的物质基础。
截止目前,保健食品备案的功能原料在辅酶Q10、鱼油、破壁灵芝孢子粉、螺旋藻和褪黑素的基础上,增加了大豆分离蛋白和乳清蛋白,共7个。此次《保健食品原料目录》的增加,更有利于生产企业针对不同的人群开发特定的产品,有利于企业扩充产品种类,进一步打开市场,促进备案制保健食品行业的发展。建议企业在产品备案前,严格按照公告中的技术要求规定,确认不同人群的使用量,提前做好规划及准备。
二、《婴幼儿配方乳粉产品配方注册管理办法》本月起正式实施
2023年6月26日,国家市场监督管理总局发布新版《婴幼儿配方乳粉产品配方注册管理办法》,将于2023年10月1日起正式实施。
新版《婴幼儿配方乳粉产品配方注册管理办法》明确了禁止变相分装、不予注册的8种情形以及现场核查和抽样检验条件;对标签标示进行了规范,包括不得使用“进口奶源”“源自国外牧场”“生态牧场”“进口原料”“原生态奶源”“无污染奶源”等模糊信息;从两方面调整了处罚力度,一是加大了对造成危害后果行为的处罚力度,二是降低了对轻微违法行为的处罚力度;此外,还优化评审机构的职责、缩短了申请时间,并从两方面提高了同一集团的资源利用率。
中食安信也对此做了更加详细的解读,请点击下方链接获取相关解读内容:
https://www.antion.net/Cn/News/viewkuaixun/id/pAmFo000ojlXRo000oacA8PctAo000oVHAO0O0OO0O0O.html
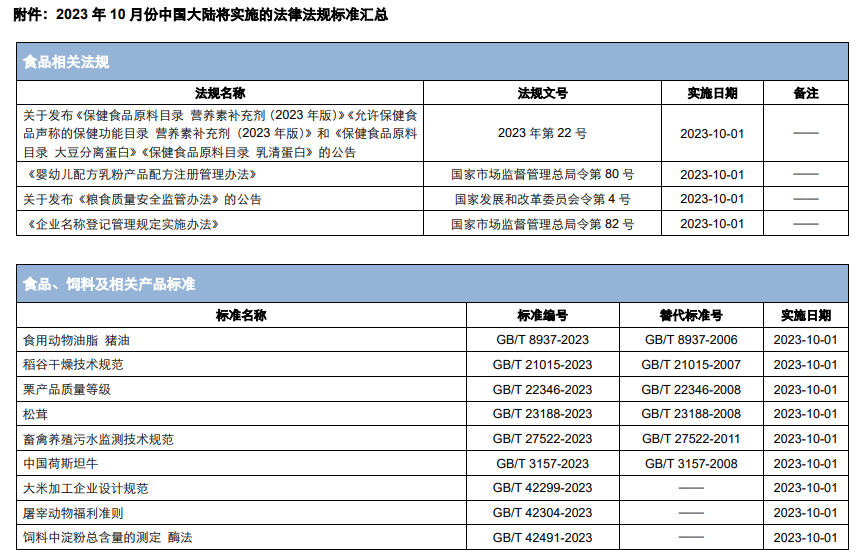
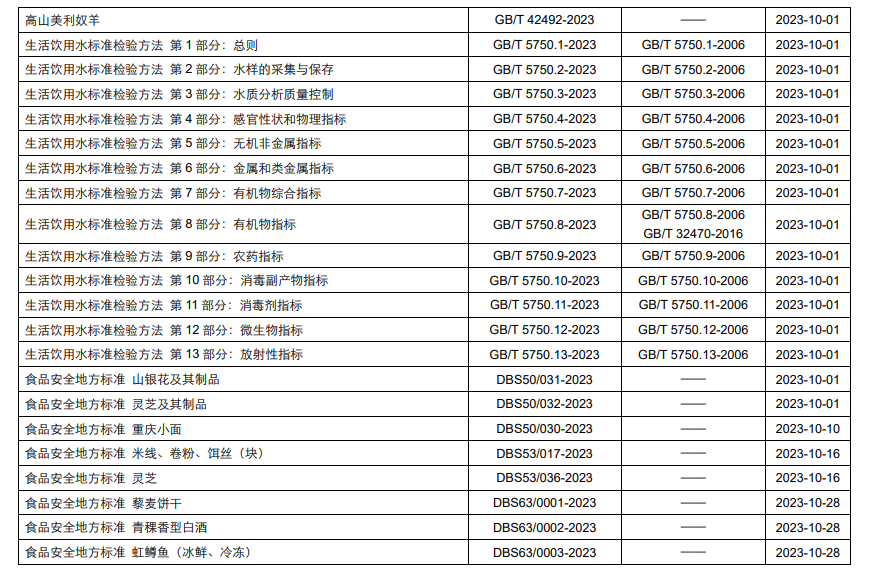
除上述法规外,中食安信还梳理汇总了10月正式实施的国家标准、地方标准等法规标准。详细内容请见附件。
 京公网安备11010502045875
京公网安备11010502045875